Avances en los sistemas de liberación de fármacos
Innovaciones en la formulación y administración de medicamentos
Los sistemas de liberación de fármacos han revolucionado la manera en que se formulan y almacenan moléculas terapéuticas. Estos sistemas optimizan la llegada de los medicamentos a las zonas específicas del organismo, maximizando la eficacia terapéutica y minimizando la acumulación no deseada en el cuerpo. Las rutas de administración son diversas, incluyendo vías oral, bucal, sublingual, nasal, oftálmica, transdérmica, subcutánea, anal, transvaginal e intravesical.
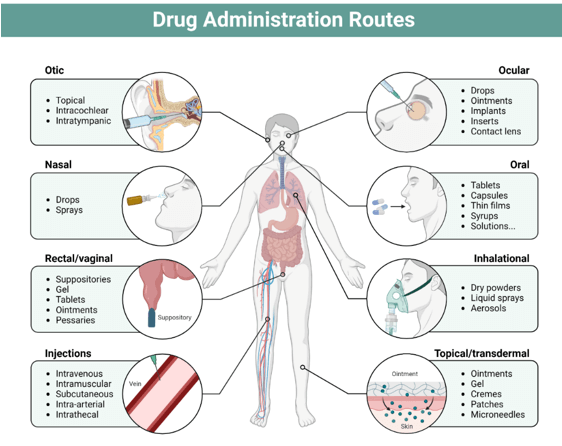
Importancia de la liberación de fármacos controlada
En las últimas décadas, estos sistemas han mejorado significativamente el tratamiento de enfermedades gracias al aumento de la circulación sistémica y al control del efecto farmacológico. La liberación controlada de fármacos, concepto establecido en la década de 1950, ha demostrado tener ventajas considerables sobre los fármacos convencionales. Liberar los fármacos a una velocidad predeterminada y durante un periodo específico asegura que no se vean afectados por las condiciones fisiológicas del organismo, lo que puede prolongar su efecto de días a años.
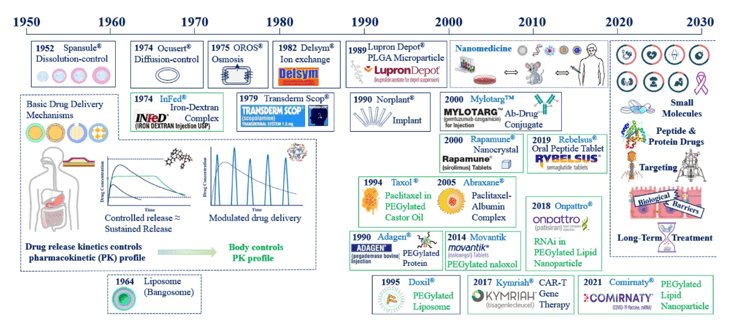
Beneficios de los sistemas de liberación de fármacos avanzados
Los sistemas de liberación controlada de fármacos mejoran la solubilidad, la acumulación en el lugar diana, la eficacia, la actividad farmacológica y las propiedades farmacocinéticas. Además, aumentan la aceptación y el cumplimiento por parte del paciente y reducen la toxicidad del fármaco.
Principales mecanismos de liberación
Recientemente, se han desarrollado varios sistemas de liberación de fármacos más avanzados, diseñados para ofrecer una liberación más cómoda, controlada y selectiva. Cada sistema de administración de fármacos tiene sus propias peculiaridades que determinan su velocidad y mecanismo de liberación. Esto se debe en gran medida a las diferencias en las características físicas, químicas y morfológicas que, en última instancia, afectarán a sus afinidades por diversas sustancias farmacológicas. Los estudios al respecto han identificado la difusión, la reacción química, la reacción del disolvente y el control de estímulos como los principales mecanismos de liberación.
Difusión controlada
Uno de los mecanismos más utilizados es la difusión. El fármaco se libera desde un depósito a través de una membrana polimérica permeable. Este método permite ajustar la velocidad de liberación controlando el grosor y la permeabilidad de la membrana. Aunque tiene ventajas como la facilidad de fabricación, uno de sus desafíos es que la tasa de liberación disminuye con el tiempo.
Activación química
La liberación activada químicamente se logra mediante una reacción química con un fármaco unido a una cadena polimérica soluble. Aunque permite altas cargas de fármaco, requiere investigación sobre la citotoxicidad del sistema. La erosión de matrices poliméricas biodegradables también es una opción, utilizando hidrólisis acuosa o enzimática.
Control por disolvente
El mecanismo de control del disolvente se basa en el hinchamiento de polímeros hidrófilos o en la osmosis. En el primer caso, al entrar en contacto con agua, las cadenas se relajan y permiten la difusión del fármaco. En el segundo, el dispositivo osmótico utiliza una membrana semipermeable que permite la entrada de agua, forzando la expulsión del fármaco.
Sistemas sensibles a estímulos
Finalmente, los sistemas sensibles a estímulos son una área prometedora, respondiendo a estímulos internos o externos para liberar el fármaco. Estos sistemas mejoran la administración de cargas a una diana específica, reduciendo la toxicidad y aumentando la eficacia.

Sistemas de liberación de fármacos actuales y aplicaciones
En los últimos años, se han logrado avances significativos en el desarrollo de sistemas de administración de fármacos basados en nanopartículas orgánicas, inorgánicas e híbridas como portadores de fármacos de acción específica. Los sistemas más recientes se han formulado con propiedades mejoradas, como un menor tamaño de partícula, mayor permeabilidad, solubilidad, eficacia, localización específica, estabilidad, toxicidad y administración sostenida. Este método de administración puede mejorar significativamente el rendimiento del agente terapéutico con respecto a las formas de dosificación convencionales.
A continuación, se muestran algunos de los distintos tipos de sistemas de liberación de fármacos, tales como:
- Liposomas
- Nanopartículas
- Dendrímeros
- Sistemas transdérmicos
- Hidrogeles
Liposomas
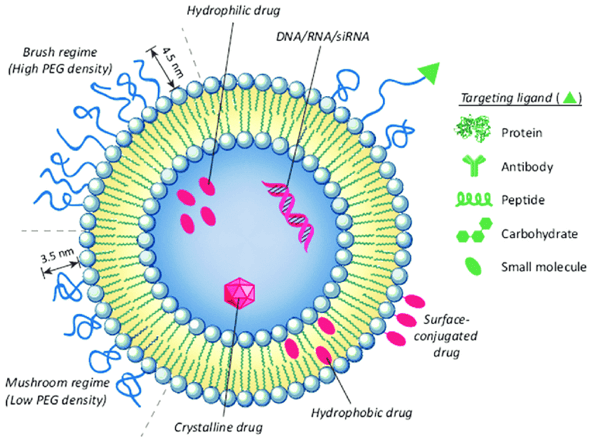
Los liposomas son vesículas sintéticas diminutas y esféricas compuestas por fosfolípidos y colesterol.
Debido a su pequeño tamaño (0.025 μm – 2.5 μm) y características hidrofílicas e hidrofóbicas, se usan como transportadores para administración de medicamentos.
Sus propiedades dependen del contenido lipídico, carga superficial, tamaño y técnica de producción.
La selección de aditivos en la bicapa afecta la tensión o fluidez, así como la carga. Los liposomas forman estructuras cerradas cuando los fosfolípidos se hidratan en soluciones acuosas.
Según la naturaleza medicinal, pueden transportar medicamentos acuosos o lipídicos en una o varias membranas bicapa. La auto agregación de lípidos polares varía según la forma molecular, temperatura y condiciones ambientales, pudiendo transformarse en partículas coloidales.
Los liposomas se han usado para administrar fármacos como paclitaxel, ciclosporina, cefepime, cabazitaxel, curcumina e ibuprofeno, mejorando su eficacia y estabilidad.
Nanopartículas
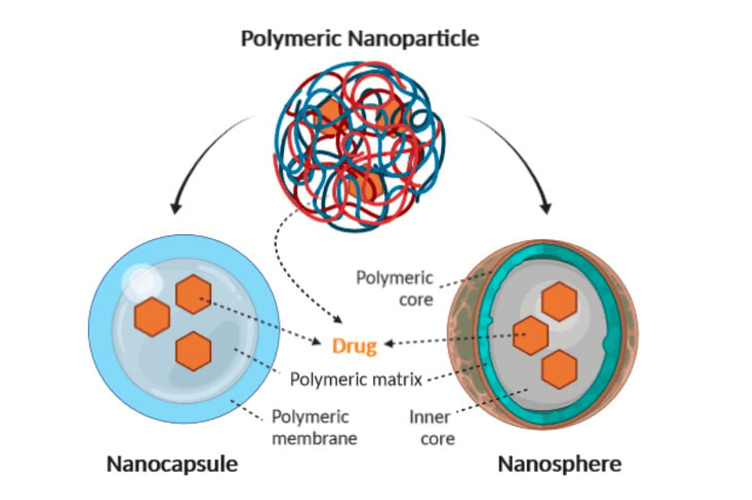
Son dispersiones de partículas con un diámetro de 10 – 1000 nm. La matriz de nanopartículas se disuelve, captura, encapsula o se une a los fármacos. Según el método de preparación, se obtienen nanopartículas, nanocápsulas o nanoesferas.
Las nanocápsulas son sistemas matriciales en los que el fármaco se distribuye física y uniformemente. Al mismo tiempo, las nanoesferas son sistemas matriciales en los que el fármaco está contenido en una cavidad rodeada por una membrana polimérica única.
Algunas de las ventajas de las nanopartículas pueden ser que mantienen y regulan la liberación del fármaco durante todo el tiempo de tránsito y en el lugar de localización, los elementos de la matriz son capaces de liberar el fármaco de forma controlada, la capacidad del fármaco es alta, y se pueden añadir ligandos dirigidos a la superficie de la partícula o aplicar una guía magnética para la localización específica del fármaco.
Microesferas
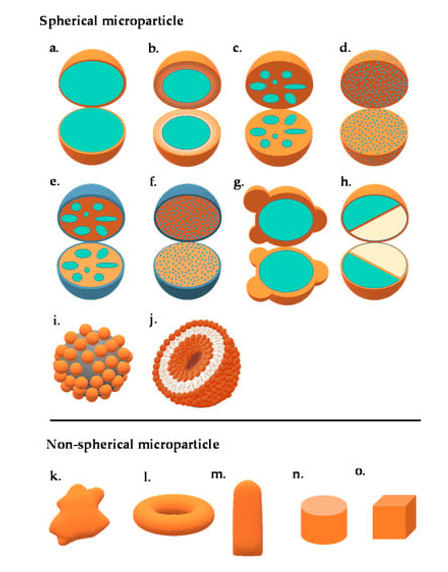
Las microesferas se definen como esferas monolíticas o agentes terapéuticos distribuidos por la matriz, ya sea como una dispersión molecular de partículas o estructuras compuestas por uno o más polímeros miscibles en una fase continua con partículas moleculares o gotitas macroscópicas.
Son partículas diminutas y esféricas con tamaños entre 1 y 1000 μm. Para prepararlas, se utilizan almidones, gomas, proteínas, grasas y ceras, que son polímeros artificiales biodegradables y materiales naturales modificados.
Los métodos de administración multiparticulados permiten una dispersión uniforme por el tracto gastrointestinal.
A diferencia de las formas farmacéuticas unitarias, la matriz polimérica no se disuelve, lo que mejora la absorción de la medicación y reduce las molestias tópicas. Por su diminuto tamaño, las microesferas se dispersan ampliamente por todo el sistema gastrointestinal, mejorando la absorción y reduciendo los efectos adversos de medicamentos irritantes para la mucosa gastrointestinal.
Dendrímeros
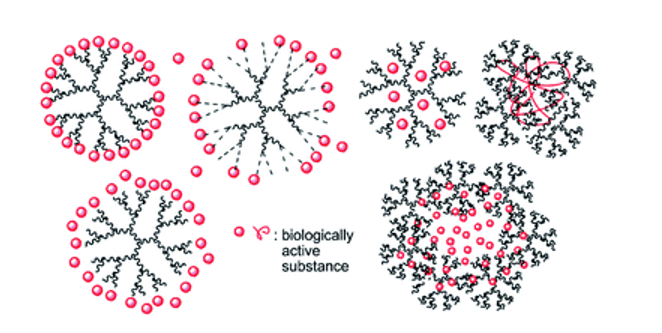
Los dendrímeros tienen una estructura dendrítica con una capa entre cada foco conocida como generación o cascada.
Permiten la administración de quimioterapéuticos, inmunoterapéuticos y paliativos a través de la barrera hematoencefálica y pueden administrar simultáneamente distintas sustancias químicas con uno o más modos de acción.
Constan de tres elementos: unidad central, dendrones ramificados y ligandos superficiales. Sus ventajas incluyen la administración directa de medicamentos en la zona afectada, utilidad en la administración selectiva, mayor permeabilidad en tumores sólidos y acumulación de macromoléculas en los tumores.
Los fármacos pueden liberarse de forma controlada y continua, diseñarse para permanecer en las capas de la piel y evitar la circulación sistémica, eludiendo el medio gastrointestinal y evitando fluctuaciones causadas por secreciones gástricas. La carga de fármaco es relativamente alta.
Hidrogeles
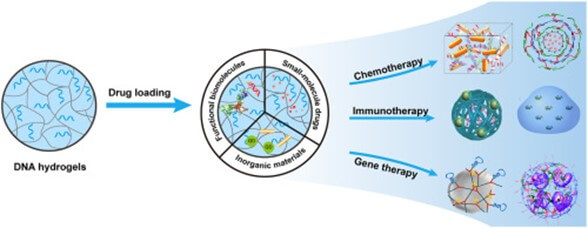
Los hidrogeles son una red polimérica tridimensional compuesta por materiales naturales y sintéticos, con una flexibilidad excepcional y alta capacidad para retener agua.
No existen en circunstancias fisiológicas, pero pueden mantener grandes volúmenes de agua o fluidos biológicos, con una consistencia gomosa similar a los tejidos vivos.
Esto los convierte en un excelente material para diversas aplicaciones, cumpliendo con los requisitos de funcionalidad, reversibilidad, estabilizabilidad y biocompatibilidad.
Poseen una elasticidad comparable a la de los tejidos reales, son biocompatibles y biodegradables, permitiendo su inyección y aplicación local. Comparados con métodos tradicionales de administración de fármacos, los hidrogeles ofrecen un efecto más sostenido y prolongado, reducen efectos secundarios, mejoran el cumplimiento terapéutico y permiten dirigir el fármaco a lugares específicos, como el colon.
Un futuro prometedor en la administración de fármacos
Perspectivas futuras
El campo de la administración de fármacos tiene un futuro brillante y apasionante. A medida que el panorama terapéutico actual se desplaza de las moléculas pequeñas a los productos biológicos, los sistemas de administración de fármacos siguen evolucionando. Se espera ver tecnologías revolucionarias capaces de mejorar la encapsulación y estabilidad de los productos biológicos, permitir su liberación sostenida durante un largo periodo de tiempo y administrarlos eficazmente a través de barreras fisiológicas complejas.
Impacto en la asistencia sanitaria global
También los futuros sistemas de administración de fármacos utilizarán materiales que se dirijan de forma más eficiente y eficaz a una biología específica, sean programables y respondan a señales biológicas, y puedan integrarse con sencillez para facilitar la traslación clínica. Las tecnologías del futuro también repercutirán en la asistencia sanitaria mundial, no sólo aumentando la precisión y eficacia de las terapias, sino también haciéndolas más asequibles y fáciles de usar.
Actualmente, la mayoría de los tratamientos novedosos, aunque curativos, sólo están al alcance de quienes pueden permitírselos. Reducir el coste sanitario de los nuevos tratamientos farmacéuticos en lugar de esperar a versiones genéricas de menor coste será de gran importancia para el público, especialmente para las personas que no tienen fácil acceso a los recursos médicos. Una serie de innovaciones y esfuerzos combinados en tecnologías de administración de fármacos y plataformas de fabricación de bajo coste altamente automatizadas proporcionarán un gran impulso hacia este objetivo, creando así equidad sanitaria.
Lectura recomendada sobre avances en biomateriales para liberación de fármacos:
Para aquellos interesados en los últimos avances en el uso de biomateriales en la liberación de fármacos, especialmente en el tratamiento del cáncer y otras terapias, les recomendamos leer el artículo «Biomaterials in Drug Delivery: Advancements in Cancer and Diverse Therapies« publicado en la revista científica MDPI. Este artículo revisa detalladamente los progresos en la encapsulación y liberación controlada de fármacos utilizando biomateriales, proporcionando una visión completa sobre cómo estas tecnologías pueden mejorar la eficacia terapéutica y reducir efectos secundarios.




